Artykuł naukowców z naszego Wydziału opublikowany w „Angewandte Chemie”
Artykuł autorstwa mgr inż. Aleksandry Rudzkiej (KBŚLiK, WCh PW), Tamary Reiter (Uniwersytet w Grazu), prof. Wolfganga Kroutila (Uniwersytet w Grazu) oraz dr. inż. Pawła Borowieckiego (KBŚLiK, WCh PW), pt.
Bienzymatic Dynamic Kinetic Resolution of Secondary Alcohols by Esterification/Racemization in Water,
został opublikowany w renomowanym czasopiśmie Angewandte Chemie International Edition (IF 16.1).
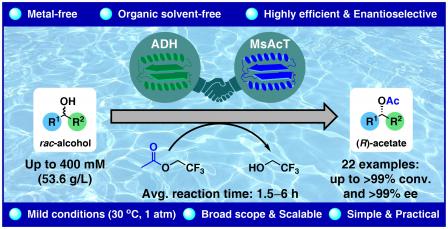
Publikacja dotyczy opracowania innowacyjnej metody biokatalitycznego dynamicznego rozdziału kinetycznego (DKR) racemicznych alkoholi drugorzędowych w środowisku wodnym. Proces ten został zrealizowany przy użyciu tandemu biokatalizatorów. Z jednej strony wykorzystano zmodyfikowaną dehydrogenazę alkoholową (ADH), która umożliwia katalityczną racemizację chiralnych alkoholi in situ poprzez mechanizm sekwencyjnej wymiany atomu wodoru pomiędzy cząsteczkami alkoholu/ketonu oraz kofaktorów NAD(P)H/NAD(P)+. Równolegle zastosowano odpowiednie stereokomplementarne warianty acylotransferazy pochodzącej z Mycobacterium smegmatis (MsAcT), które katalizują enancjoselektywną transestryfikację alkoholi z wykorzystaniem octanu 2,2,2-trifluoroetylu w wodzie, biegnącą wbrew niekorzystnej termodynamice dla tego typu układów reakcyjnych.
Warto podkreślić, że opracowany przez zespół dr Borowieckiego dwuenzymatyczny proces kaskadowy deracemizacji chiralnych alkoholi stanowi przełomowe rozwiązanie problemów syntetycznych, które przez ponad 30 lat stanowiły wyzwanie dla środowiska chemików bioorganików. Dotychczasowe chemoenzymatyczne procesy DKR opierały się na zastosowaniu lipaz oraz kosztownych i niestabilnych kompleksów metali grup przejściowych. Z tego względu ich realizacja wymagała bezwodnych i beztlenowych warunków reakcyjnych, wysokich temperatur i toksycznych zasad do aktywacji kompleksów metali oraz użycia lotnych, szkodliwych dla środowiska rozpuszczalników organicznych.
Dodatkowo praktyczne zastosowanie tych metod było utrudnione przez relatywnie długie czasy reakcji, powstawanie licznych produktów ubocznych, wzajemną dezaktywację katalizatorów DKR, konieczność immobilizacji enzymów, ograniczone spektrum substratowe oraz skomplikowane procedury izolacji i oczyszczania produktów.
Zaprojektowany przez naszych naukowców dwuenzymatyczny DKR realizowany jest przy użyciu w pełni biodegradowalnych biokatalizatorów w wodnych roztworach buforowych. Proces przebiega w łagodnych warunkach temperaturowych i pH, z bardzo wysokimi wydajnościami oraz nadmiarami enancjomerycznymi dla izolowanych produktów, a czas trwania reakcji został drastycznie zredukowany nawet do zaledwie 1,5 godziny.
Badania opisane na łamach Angewandte z pewnością przyczynią się do rozwoju wydajniejszych, bardziej selektywnych oraz proekologicznych metod syntezy optycznie czynnych związków o wysokiej wartości dodanej.
Prace zostały sfinansowane przez Narodowe Centrum Nauki (NCN) w ramach grantu OPUS 24 (nr 2022/47/B/ST4/00139).
Więcej informacji dostępne jest na stronie czasopisma: https://onlinelibrary.wiley.com/doi/10.1002/anie.202420133.